 |
تفاعلات التأكسد والاختزال الذاتي
Disproportionation Reaction
تفاعل التأكسد والاختزال الذاتي: سلوك المادة كعامل مؤكسد وكعامل مختزل في التفاعل نفسه.
مثال:
يحدث تفاعل التأكسد والاختزال الذاتي التالي عند إمرار الكلور في محلول قاعدي:
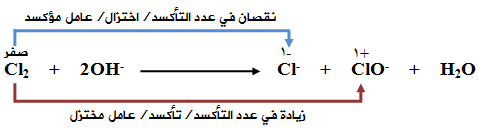
في التفاعل السابق يعتبر Cl2 عاملاً مؤكسداً ومختزلاً لأنه تعرض للتأكسد وللاختزال في التفاعل نفسه، لذا يسمى هذا التفاعل تفاعل تأكسد واختزال ذاتي.
سؤال 1 :
وضح التأكسد والاختزال الذاتي في المعادلة التالية:
2H2O2 → 2H2O + O2
سؤال 2 :
ادرس التفاعلات التالية، ثم أجب عن الأسئلة التي تليها:
P4 → a) PH3 + H2PO2-
Se → b) Se2- + SeO32-
Br2 → c) Br- + BrO3-
1- بيّن أن التفاعلات السابقة تمثل تفاعلات تأكسد واختزال ذاتي.
2- ما التغير في عدد تأكسد كل من الفسفور، والسيلينيوم، والبروم عند تأكسدها؟
إجابات اسئلة الدرس في الملفات المرفقة.