 |
طاقة التنشيط والتغير في المحتوى الحراري
تقسم التفاعلات حسب الطاقة إلى قسمين:
- تفاعلات تحتاج إلى طاقة لكي تحدث، وتسمى تفاعلات ماصة للطاقة.
- تفاعلات تنتج طاقة عندما تحدث، وتسمى تفاعلات طاردة للطاقة.
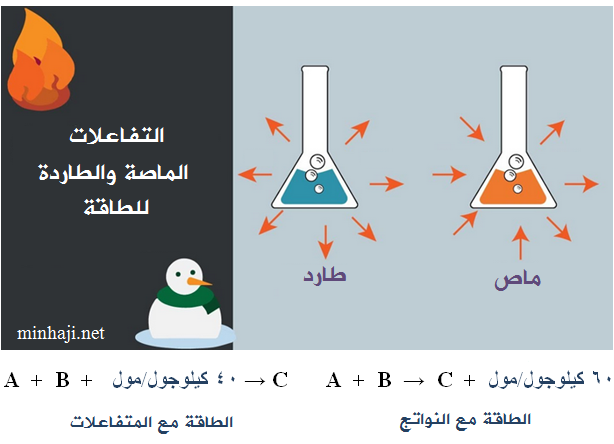
ويمكن التعبير عن التفاعل الماص والطارد باستخدام المحتوى الحراري (∆H) أو (طاقة التفاعل)، ويمثل المحتوى الحراري للتفاعل الفرق بين طاقة وضع المواد الناتجة وطاقة وضع المواد المتفاعلة.
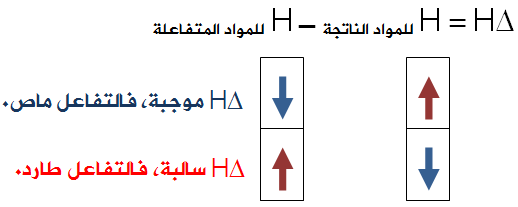
وليس لـ H∆ علاقة بسرعة التفاعل، ولكن سرعة التفاعل تتأثر عكسياً بطاقة التنشيط.
منحنى التفاعل الماص للطاقة:
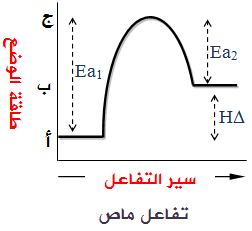
أ : طاقة وضع المواد المتفاعلة.
ب : طاقة وضع المواد الناتجة.
ج: طاقة وضع المعقد المنشط.
Ea1 : طاقة التنشيط للتفاعل الأمامي. ( Ea1 = طاقة وضع المعقد المنشط - طاقة وضع المتفاعلات )
Ea2 : طاقة التنشيط للتفاعل العكسي. ( Ea2 = طاقة وضع المعقد المنشط - طاقة وضع النواتج )
H∆ : المحتوى الحراري للتفاعل. ( H∆ = طاقة وضع النواتج - طاقة وضع المتفاعلات )
منحنى التفاعل الطارد للطاقة:
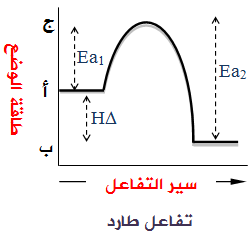
في التفاعلات الماصة يكون:
- طاقة وضع المواد الناتجة أعلى من طاقة وضع المواد المتفاعلة.
- قيمة H∆ موجبة.
- التفاعل العكسي أسهل حدوثاً وأسرع من التفاعل الأمامي، لأن طاقة التنشيط للتفاعل العكسي أقل من طاقة التنشيط للتفاعل الأمامي.
- Ea1 = Ea2 + H∆ .
في التفاعلات الطاردة يكون:
- طاقة وضع المواد الناتجة أقل من طاقة وضع المواد المتفاعلة.
- قيمة H∆ سالبة.
- التفاعل الأمامي أسهل حدوثاً وأسرع من التفاعل العكسي، لأن طاقة التنشيط للتفاعل الأمامي أقل من طاقة التنشيط للتفاعل العكسي.
- Ea2 = Ea1 + H∆
سؤال 1 :
تمعن الشكل التالي والذي يمثل تصادم A مع B لإنتاج AB ، ثم أجب عن الأسئلة التي تليه.
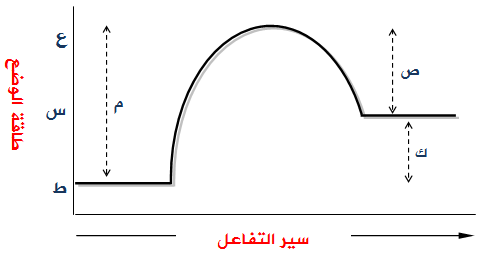
- ما الرمز الذي يمثل طاقة كل من: المواد المتفاعلة، والمواد الناتجة، والمعقد المنشط؟
- هل التفاعل ماص أم طارد للطاقة؟ لماذا؟
- ماذا تمثل كل من الرموز: ص، ك، م؟
سؤال 2 :
تمعن الشكل التالي والذي يمثل تفاعل F2 مع H2 لإنتاج HF ، ثم أجب عن الأسئلة التي تحاذيه.
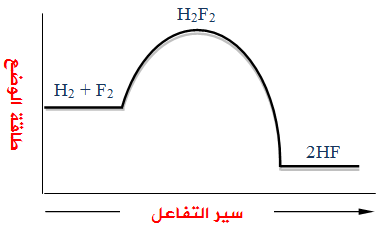
- هل التفاعل ماص أم طارد للطاقة؟
- أيها أسهل حدوثاً: تكوّن HF أم تفككه؟
- ما صيغة المعقد المنشط؟
سؤال 3 :
المخطط المجاور يمثل سير التفاعل للتفاعل العام: A + B → C ، حدد من خلال الرسم قيمة كل من:
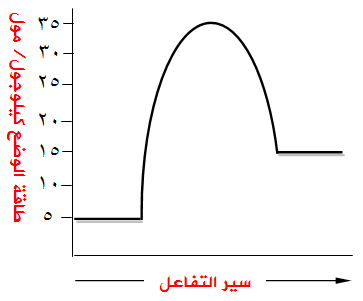
- طاقة وضع المواد المتفاعلة.
- طاقة وضع المواد الناتجة.
- H∆ للتفاعل.
- طاقة التنشيط للتفاعل الأمامي.
- طاقة التنشيط للتفاعل العكسي.
- طاقة المعقد المنشط.
سؤال 4 :
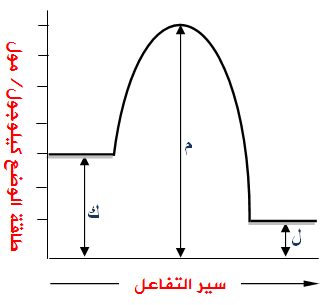
يمثل الشكل الآتي العلاقة بين سير التفاعل وطاقة الوضع بوحدة الكيلوجول/مول، عبّر عن مقدار كل مما يلي باستخدام الرموز (ك ، ل ، م) المبينة في الشكل:
-
-
- طاقة وضع المتفاعلات.
- طاقة وضع النواتج.
- المحتوى الحراري للتفاعل.
- طاقة المعقد المنشط.
- طاقة التنشيط للتفاعل الأمامي.
- طاقة التنشيط للتفاعل العكسي.
-
سؤال 5 :
في التفاعل الافتراضي الآتي: 2A + B → 2C ، إذا علمت أنّ:
- طاقة الوضع للمواد المتفاعلة = 240 كيلو جول.
- طاقة الوضع للمواد الناتجة = 20 كيلو جول.
- طاقة التنشيط للتفاعل الأمامي = 10 كيلو جول ، أجب عما يأتي:
- ما قيمة طاقة التنشيط للتفاعل العكسي؟
- ما قيمة طاقة الوضع للمعقد المنشط؟
- ما أثر زيادة درجة الحرارة على قيمة طاقة التنشيط للتفاعل الأمامي (تزداد ، تقل ، تبقى ثابتة)؟
سؤال 6 :
إذا كانت قيم طاقات الوضع (كيلوجول) لتفاعل افتراضي هي:
المواد المتفاعلة 80، المواد الناتجة 50، طاقة التنشيط للتفاعل الأمامي 75، فأجب عن الأسئلة الآتية:
- ما قيمة طاقة التنشيط للتفاعل العكسي؟
- ما طاقة وضع المعقد المنشط؟
- ما قيمة H∆ للتفاعل؟
سؤال 7 :
إذا كان لديك التفاعل التالي: 40 كيلوجول/مول + A(g) + B(g) → AB(g)
وكانت قيمة طاقة الوضع للمعقد المنشط للتفاعل السابق = 130 كيلوجول/مول، وطاقة التنشيط للتفاعل العكسي = 100 كيلوجول/مول، فأجب عن الأسئلة التالية:
- ما قيمة طاقة التنشيط للتفاعل الأمامي؟
- ما قيمة طاقة وضع المواد المتفاعلة؟
- ما قيمة طاقة وضع المواد الناتجة؟
- ما قيمة المحتوى الحراري للتفاعل متضمناً الإشارة؟
- أيهما أسهل حدوثاً: تفكك AB أم تكونه؟