 |
أسئلة المحتوى وإجاباتها
الروابط الكيميائية وأنواعها
أتحقق صفحة (62):
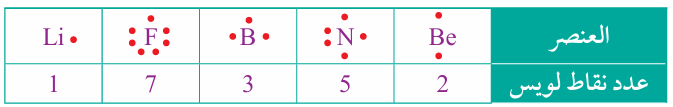
أكتب تركيب لويس لكل من ذرات العاصر في الجدول الآتي:
|
العنصر |
Li |
F |
B |
N |
Be |
|
العدد الذري |
3 |
9 |
5 |
7 |
4 |
أفكر صفحة (64):
يرتبط الألمنيوم (AI) بالكبريت (S)؛ لتكوين مركب (Al2S3)، فكيف يحدث ذلك؟
13Al:1s2 2s2 2p6 3s2 3p1
16S:1s2 2s2 2p6 3s2 3p4
ذرة Al تفقد ثلاثة إلكترونات من المستوى الخارجي، فينتج Al3+
ذرة S تكتسب إلكترونين من المستوى الخارجي، فينتج S2-
بما أن عدد الإلكترونات المفقودة يساوي عدد الإلكترونات المكتسبة فإنه يلزم وجود ثلاثة أيونات S2- لتكتسب ستة إلكترونات من أيونين من Al3+؛ لذا يرتبط أيونان من Al3+ بثلاثة أيونات من S2-.
أتحقق صفحة (64):
ما المقصود بالرابطة الأيونية؟
الرابطة الأيونية: القوة التي تجذب الأيونات ذات الشحنات المختلفة في المركبات، وهي تنشأ بين ذرات الفلزات واللافلزات.
الشكل 1 صفحة (64):
الترابط بين ذرتي الصوديوم والكلور.
أفسر أثر طاقة تأين ذرة Na وذرة Cl في تكوين الأيون الموجب والأيون السالب.
11Na: [Ne] 3s1
طاقة تأين ذرة Na منخفضة؛ لذا يسهل أن تفقد إلكتروناً واحداً، فينتج Na+ .
17Cl: [Ne] 3s2 3p5
طاقة تأين ذرة Cl مرتفعة؛ لذا لا تميل إلى فقدات الإلكترونات، وإنما تميل لكسب الإلكترونات، فتكسب إلكتروناً واحداً، فينتج Cl- .
أتحقق صفحة (67):
ما المقصود بكل من الروابط التساهمية الأحادية، والثنائية، والثلاثية؟
الرابطة التساهمية الأحادية: رابطة تنشأ عن تشارك ذرتين بزوج واحد من الإلكترونات.
الرابطة التساهمية الثنائية: رابطة تنشأ عن تشارك ذرتين بزوجين من الإلكترونات.
الرابطة التساهمية الثلاثية: رابطة تنشأ عن تشارك ذرتين بثلاثة أزواج من الإلكترونات.
الشكل 9 صفحة (67):
الرابطة التساهمية الثلاثية في جزي N2
أذكر عدد أزواج الإلكترونات غير الرابطة على ذرة N الواحدة.
كل ذرة N تمتلك زوجاً واحداً من الإلكترونات غير الرابطة.
أفكر صفحة (67):
أوضح كيف تتكون الروابط في جزيء HCN؟
ذرة H لديها إلكترون تكافؤ واحد، وذرة C لديها أربعة إلكترونات تكافؤ، وذرة N لديها خمسة إلكترونات تكافؤ؛ لذا تتشارك ذرة H بإلكترونها مع إلكترون من ذرة C؛ أي تتشارك الذرتان بزوج من الإلكترونات، ويبقى لدى ذرة C ثلاثة إلكترونات تتشارك بها مع ثلاثة إلكترونات من ذرة N، وبذلك تتشارك ذرتا C و N بثلاثة أزواج من الإلكترونات.
ويمكن تمثيل روابط الجزيء على النحو الآتي:
H – C ≡ N
أتحقق صفحة (68):
ما المقصود بالرابطة الفلزية؟
الرابطة الفلزية: قوة تجاذب بين الأيونات الموجبة للفلزات والإلكترونات حرة الحركة في الشبكة البلورية.