 |
مفهوم المول
The Mole Concept

نستخدم في تعبيراتنا الكثير من الكلمات التي تعبر عن الأعداد، فمثلاً نقول زوجٌ من الأحذية، قرنٌ من الزمان، وعقدٌ من السنوات، ودزينة من الدفاتر وغيرها.
يستخدم في الكيمياء تعبير المول ويعني 6.022 × 2310 ذرة أو أيون أو جزيء أو إلكترون وغيرها.
يسمى العدد 6,022 × 2310 بعدد أفوجادرو نسبة إلى العالم الإيطالي أماديو أفوجادرو.
فلو كان لديك مولاً واحداً من ذرات الحديد فهذا يعني أن لديك 6.022 × 2310 ذرة حديد.
ولو كان لديك مولاً واحداً من جزيئات الأكسجين فهذا يعني أن لديك 6.022 × 2310 جزيء أكسجين وهكذا.
الكتلة المولية
هب أن هناك متجراً يبيع مواد كيمياوية وطُلب منك أن تشتري مولاً من ذرات الصوديوم، فما عدد ذرات الصوديوم التي على التاجر أن يعدها لك لتحصل على طلبك؟
بالتأكيد سيعد لك 6,022 × 2310 ذرة صوديوم، والأمر غاية في الصعوبة، لذا تم استخدام مفهوم الكتلة المولية.
تسمى كتلة المول الواحد من المادة الكتلة المولية.
في حالة الذرات تساوي الكتلة المولية الكتلة الذرية للعنصر.
في حالة الجزيئات تساوي الكتلة المولية الكتلة الجزيئية للجزيء.
مثال (1):
إذا كان لديك مول من ذرات الصوديوم، فما كتلته المولية، وما عدد ذرات الصوديوم في المول الواحد منه.
الكتلة الذرية للصوديوم = 23 وحدة كتل ذرية.
وهذا يعني أن:
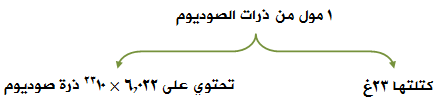
مثال (2):
إذا كان لديك مول من جزيئات غاز ثاني أكسيد الكربون CO2 ، فما كتلتها المولية، وما عدد جزيئات ثاني أكسيد الكربون في المول الواحد منها؟
الكتلة الذرية للكربون = 12
الكتلة الذرية للأكسجين = 16
الحل:
لحساب الكتلة المولية لمول واحد من غاز CO2 نحسب الكتلة الجزيئية له:
الكتلة الجزيئية = (عدد ذرات الكربون × كتلته الذرية) + (عدد ذرات الأكسجين × كتلته الذرية)
الكتلة الجزيئية = (1 × 12) + (2 × 16)
الكتلة الجزيئية = (12) + (32) = 44 وحدة كتل جزيئية.
الكتلة الجزيئية = الكتلة المولية = 44غ/مول.
ماذا يعني أن تكون الكتلة المولية لثاني أكسيد الكربون تساوي 44 ؟
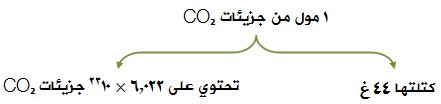
سؤال:
بالرجوع إلى قيم الكتل الذرية في الجدول الدوري احسب الكتل المولية للماء H2O .
الحل:
الكتلة المولية للماء = (عدد ذرات الهيدروجين × كتلته الذرية) + (عدد ذرات الأكسجين × كتلته الذرية)
الكتلة المولية للماء = (2 × 1) + (1 × 16) = 18 غ/مول.