عدد التأكسد
Oxidation number
عدد التأكسد في المركبات الأيونية: الشحنة الفعلية لأيون الذرة.
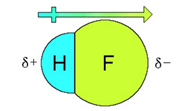 عدد التأكسد في المركبات الجزيئية: الشحنة التي ستكسبها الذرة فيما لو أعطيت إلكترونات الرابطة كلياً للذرة الأعلى كهرسلبية.
عدد التأكسد في المركبات الجزيئية: الشحنة التي ستكسبها الذرة فيما لو أعطيت إلكترونات الرابطة كلياً للذرة الأعلى كهرسلبية.
قواعد حساب عدد التأكسد
- عدد تأكسد العناصر الحرة (ذرات أو جزيئات) يساوي صفراً مثل:S8 ، O2 ، P4 ، H2 ، Cl2 ، Mg .
- عدد التأكسد في الأيون أحادي الذرة يساوي شحنة الأيون.
أمثلة:
عدد تأكسد المغنيسيوم في أيون Mg2+ هو (+2).
عدد تأكسد النيتروجين في أيون N3- هو (-3).
- عدد تأكسد الفلزات في مركباتها دائماً موجب، لأنها تميل دائماً لفقد الإلكترونات.
- عدد تأكسد عناصر المجموعة الأولى (القلويات) في مركباتها دائماً (+1).
- عدد تأكسد عناصر المجموعة الثانية (القلويات الترابية) في مركباتها دائماً (+2).
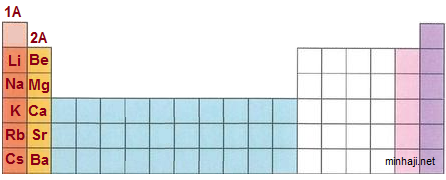
- عدد تأكسد الألمنيوم في مركباته (+3).
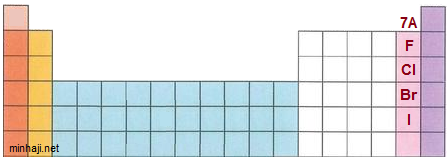
- عدد تأكسد الهالوجينات (المجموعة VIIA) يساوي (-1) في المركبات الأيونية.
( مثل: NaCl ، AlBr3 ، MgI2 ).
ويكون موجباً في المركبات التي تحتوي على أكسجين مثل: HOCl
أما الفلور فيكون عدد تأكسده (-1) في جميع مركباته.
- عدد تأكسد الأكسجين في مركباته غالباً (-2)،
مثل: الماء H2O ، وأكسيد الصوديوم Na2O .
باستثناء حالتين:
أ- (-1) في فوق الأكاسيد.
مثل: فوق أكسيد الهيدروجين H2O2 ، فوق أكسيد الصوديومNa2O2 .
ب- (+2) إذا اتحد الأكسجين مع الفلور في المركب OF2 ، و (+1) في المركب O2F2 ، ويكون عدد تأكسده موجباً لأن الفلور أعلى الذرات كهرسلبية في الجدول الدوري لذا فهو دائماً سالب الشحنة.
- عدد تأكسد الهيدروجين في مركباته غالباً (+1).
باستثناء هيدريدات الفلزات فهو (-1).
أمثلة: هيدريد الصوديوم NaH ، هيدريد الكالسيوم CaH2 ، هيدريد الليثيوم والألمنيوم LiAlH4 .
10- مجموع أعداد التأكسد للذرات في المركب المتعادل يساوي صفراً .
مثال: مجموع أعداد تأكسد النيتروجين والهيدروجين والأكسجين في المركب HNO3 يساوي صفراً.
11- مجموع أعداد التأكسد للأيون عديد الذرات يساوي شحنة الأيون مقداراً وإشارةً.
مثال: مجموع أعداد تأكسد الكروم والأكسجين في الأيون CrO42- يساوي (-2).
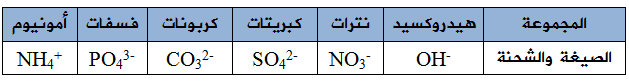
12- أهم المجموعات عديدة الذرات وأعداد تأكسدها:
سؤال 1 :
احسب عدد تأكسد الكبريت في حمض الكبريتيك H2SO4 .
الحل:
(عدد تأكسد S × عدد ذراته ) + (عدد تأكسد O × عدد ذراته) + (عدد تأكسد H × عدد ذراته) = صفر
(س × 1) + (-2×4) + (+1×2) = صفر
عدد تأكسد الكبريت = +6
سؤال 2 :
احسب عدد تأكسد الكبريت في الأيون: S2O32- .
الحل:
(عدد تأكسد S × عدد ذراته ) + (عدد تأكسد O × عدد ذراته) = -2
(س × 2) + (-2×3) = -2
(2س) + (-6) = -2
عدد تأكسد الكبريت = +2
سؤال 3 :
احسب عدد تأكسد اليود I في الأيون: IO4-.
الحل:
(عدد تأكسد I × عدد ذراته ) + ( عدد تأكسد O × عدد ذراته ) = -1
(1 × س) + (-2×4) = -1
عدد تأكسد اليود = +7
سؤال 4 :
احسب عدد تأكسد اليود I في الأيون: H3IO62-.
(عدد تأكسد I × عدد ذراته) + (عدد تأكسد O × عدد ذراته) + (عدد تأكسد H × عدد ذراته) = -2
(س × 1) + (-2×6) + (+1×3) = -2
(س) + (-12) + (+3) = -2
(س) + (-9) = -2
عدد تأكسد اليود = +7
سؤال 5 :
ما عدد تأكسد الكبريت (S) في المركبات والأيونات التالية:
HSO3- ، Na2S ، KHSO4 ، S2O62- ، S2- ، HS- ، Na2S2O7 ، SF2
سؤال 6 :
ما عدد تأكسد الأكسجين (O) في المركبات والأيونات التالية:
Cr2O72- ، OF2 ، MgO2 ، CaO ، O2- ، O2F2 ، O3
سؤال 6 :
ما عدد تأكسد الهيدروجين (H) في المركبات والأيونات التالية:
CaH2 ، H2 ، HSO4- ، KH ، HF
سؤال 7 :
- ما عدد تأكسد كل من الحديد والنيتروجين في نترات الحديد Fe(NO3)3 ؟
- ما عدد تأكسد كل من الكروم والنيتروجين في كرومات الأمونيوم (NH4)2Cr2O7 ؟
سؤال 8 :
- ما عدد تأكسد الكروم Cr في كلٍ من: CrO2- ، CrO3 ، Cr2O72-؟
- ما عدد تأكسد المنغنيز Mn في كلٍ من: MnO2 ، MnO4-؟
- ما عدد التأكسد للعنصر الذي تحته خط في كلٍ مما يأتي؟
VO3- ، AsO43- ، P2O5 ، Li4C ، BF3 ، KClO3 ، KH2PO4
سؤال 9 : أسئلة موضوعية وزارية
- عدد تأكسد الكروم ( Cr ) في الصيغة الكيميائية Cr2O72- :
أ) (-2) ب) (+2) ج) (+6) د) (+7)
- عدد تأكسد الكبريت ( S ) في الأيون S2O32- يساوي:
أ) (+2) ب) (+3) ج) (+4) د) (-4)
- عدد تأكسد اليود في الأيون H3IO62- يساوي:
أ) (+7) ب) (-7) ج) (+1) د) (-1)
- عدد تأكسد (As) في الأيون AsO43- يساوي:
أ) (+3) ب) (-3) ج) (-5) د) (+5)
- عدد تأكسد الكبريت ( S ) يساوي (+2) في:
أ) HSO3- ب) S2O32- ج) HS- د) Na2S
- رقم تأكسد الهيدروجين في المركب ( BaH2 ) يساوي:
أ) -1 ب) +1 ج) +2 د) -2
- عدد تأكسد الأكسجين في المركب OF2 يساوي:
أ) (-2) ب) (-1) ج) (+1) د) (+2)
- المركب الذي يكون عدد تأكسد الأكسجين فيه (-1) هو:
أ) OF2 ب) Cl2O ج) H2O2 د) MgO
- عدد تأكسد اليود في IO3- هو:
أ) +1 ب) +3 ج) +4 د) +5
- أعلى عدد تأكسد للنيتروجين يكون في:
أ) N2H4 ب) NH3 ج) NO2- د) NO3-
- عدد تأكسد الهيدروجين يساوي (-1) في المركب:
أ) H2O ب) HCl ج) NaH د) HF
إجابات أسئلة الدرس في الملفات المرفقة
إعداد : أ. أحمد الحسين
26 / 10 / 2019
النقاشات