إجابات أسئلة مراجعة الدرس الثاني
الخلايا الجلفانية
السؤال الأول:
الفكرة الرئيسة: كيف تنتج الخلية الجلفانية الطاقة الكهربائية؟
تنتج الخلية الجلفانية الطاقة الكهربائية من خلال تفاعل تأكسد واختزال تلقائي الحدوث؛ إذ يحدث التأكسد عند قطب المصعد وتنتقل الإلكترونات عبر الأسلاك باتجاه قطب المهبط وتحدث عنده عملية الاختزال.
السؤال الثاني:
أوضح المقصود بكل من:
- القنطرة الملحية.
- جهد الاختزال المعياري.
القنطرة الملحية: أنبوب زجاجي على شكل حرف (U) يحتوي على محلول مشبع لأحد الأملاح، يصل بين نصفي الخلية الجلفانية؛ ويحافظ على شحناتها الكهربائية.
جهد الاختزال المعياري: مقياس لميل نصف تفاعل الاختزال للحدوث في الظروف المعيارية.
السؤال الثالث:
خلية جلفانية يحدث فيها التفاعل الآتي:
Co + Cu2+ → Co2+ + Cu
أ- أحدد فيها المصعد والمهبط.
المصعد: Co ، والمهبط: Cu
ب- أكتب نصفي تفاعل التأكسد والاختزال.
نصف تفاعل التأكسد: Co → Co2+ + 2e-
نصف تفاعل الاختزال: Cu2+ + 2e- → Cu
ج- أحسب جهد الخلية المعياري، وأكتب تعبيراً رمزياً للخلية الجلفانية.
E0cell = E0(cathode) – E0(anode)
E0cell = + 0.34 – (- 0.27) = + 0.61 V
أكتب تعبيراً رمزياً للخلية الجلفانية:
Cu(s)│Cu2+(aq) ││ Co2+(aq)│Co(s)
د- ما التغير الذي يحدث لكتلة كلا القطبين؟
تقل كتلة الكوبالت، وتزداد كتلة قطب النحاس.
السؤال الرابع:
نصفا التفاعل الآتيان يشكلان خلية جلفانية في الظروف المعيارية:
I2 (s) + 2e- → 2I- Eo = 0.54 V
Fe2+ (aq) + 2e- → Fe (s) Eo = - 0.44 V
أجيب عن الأسئلة الآتية المتعلقة بهما:
أ- أكتب معادلة التفاعل الكلي في الخلية.
Fe + I2 → Fe2+ + 2I-
ب- أحسب جهد الخلية المعياري.
Eocell = Eo(cathode) – Eo(anode)
Eocell = + 0.54 – (- 0.44) = + 0.98 V
ج- ما التغير الذي يحدث لتركيز أيونات كل من I- و Fe2+ ؟
يزداد تركيز أيونات Fe2+ ، ويزداد تركيز أيونات I- .
د- أكتب رمز الخلية الجلفانية.
Fe(s)│Fe2+(aq) ││ I2(s)│I-(aq) │Pt
السؤال الخامس:
 أدرس الجدول الآتي، الذي يوضح جهد الخلية المعياري لعدد من الخلايا الجلفانية المكونة من الفلزات ذوات الرموز (A,B,C,D,E)، وجميعها تكون أيونات ثنائية موجبة، ثم أجيب عن الأسئلة الآتية:
أدرس الجدول الآتي، الذي يوضح جهد الخلية المعياري لعدد من الخلايا الجلفانية المكونة من الفلزات ذوات الرموز (A,B,C,D,E)، وجميعها تكون أيونات ثنائية موجبة، ثم أجيب عن الأسئلة الآتية:
أ- أحدد الفلز الذي له أعلى جهد اختزال معياري: D أم C .
D
ب- أحدد أقوى عامل مؤكسد.
A2+
ج- أتنبأ: هل يمكن تحريك محلول نترات E بملعقة من A ؟ أفسر إجابتي.
يمكن تحريك المحلول.
التفاعل المراد التنبؤ بحدوثه:
A + E(NO3)2 → E + A(NO3)2
بما أن جهد اختزال A أعلى من جهد اختزال E ؛ إذن التفاعل السابق لا يحدث بشكل تلقائي.
د- أحدد اتجاه حركة الإلكترونات عبر الأسلاك في الخلية الجلفانية المكونة من نصف خلية E2+│E ونصف خلية D│D2+ .
تتحرك الإلكترونات من قطب E إلى قطب D .
هـ- أحسب جهد الخلية المعياري للخلية الجلفانية المكونة من نصف خلية C│C2+ ونصف خلية B│B2+ .
1.9 V
السؤال السادس:
فلزان أعطيا الرموز الافتراضية A و B ، قيست جهود الاختزال المعيارية لنصفي الاختزال المعياريين المكونين لخلية جلفانية كالآتي:
A3+ + e- → A2+ Eo = 0.77 V
B+ + e- → B Eo = 0.80 V
أ- أكتب معادلة كيميائية للتفاعل الكلي في الخلية الجلفانية.
A2+ + B+ → A3+ + B
ب- أحسب Eo للتفاعل الكلي.
Eocell = Eo(cathode) – Eo(anode)
Eocell = + 0.80 – (0.77) = + 0.03 V
ج- أحدد العامل المؤكسد والعامل المختزل في التفاعل.
العامل المؤكسد: B+ ، العامل المختزل: A2+
السؤال السابع:
أدرس الجدول المجاور الذي يمثل جهود الاختزال المعيارية لبعض المواد، ثم أجيب عن الأسئلة الآتية:
 أ- أحدد أقوى عامل مؤكسد وأقوى عامل مختزل.
أ- أحدد أقوى عامل مؤكسد وأقوى عامل مختزل.
أقوى عامل مؤكسد: Br2 ، أقوى عامل مختزل: Mn
ب- أستنتج. هل يمكن حفظ محلول البروم Br2 في وعاء من الفضة؟ أفسر إجابتي.
التفاعل المراد التنبؤ بحدوثه:
Ag + Br2 → Ag+ + 2Br-
Eocell = Eo(cathode) – Eo(anode)
Eocell = + 1.06 – (0.80) = + 0.26 V
جهد التفاعل موجب، فالتفاعل قابل للحدوث؛ إذن لا يمكن حفظ البروم في وعاء من الفضة.
ج- أقارن. ما الفلزين اللذين يكونان خلية جلفانية لها أكبر جهد خلية معياري؟.
Ag / Mn
د- أستنتج المادة التي تستطيع أكسدة Cd ولا تؤكسد Pb .
Co
هـ- أحدد القطب الذي تزداد كتلته في الخلية الجلفانية (Cd-Pb).
Pb
و- أحدد الفلز الذي لا يحرر غاز الهيدروجين من محلول حمض HCl المخفف.
Ag
ز- في الخلية الجلفانية التي أعطيت الرمز الآتي:
Co(s)│Co2+(aq)││Sc3+(aq)│Sc(s)
إذا علمت أن جهد الخلية المعياري Eocell = 1.8 V ، فأجيب عن الأسئلة الآتية:
أ- أحدد اتجاه حركة الإلكترونات عبر الأسلاك في الخلية.
من قطب Sc إلى قطب Co .
ب- أحسب جهد الاختزال المعياري لقطب السكانديوم Sc .
Eocell = E0(cathode) – Eo(anode)
1.8 = - 0.28 – (Eo(Sc))
EoSc = - 2.08 V
ج- أكتب معادلة التفاعل الكلي في الخلية.
2Sc + 3Co2+ → 2Sc3+ + 3Co
السؤال الثامن:
أختار الإجابة الصحيحة لكل فقرة من الفقرات الآتية:
1. العبارة الصحيحة المتعلقة بالخلية الجلفانية التي تفاعلها: Mg + Ni2+ → Mg2+ + Ni هي:
أ. القطب الموجب Mg.
ب. في نصف الخلية Mg2+ | Mg يقل تركيز أيونات Mg2+.
ج. القطب Ni هو المصعد.
د. يقل تركيز أيونات Ni2+ في نصف الخلية Ni2+ | Ni.
2. العبارة الصحيحة اعتمادًا على جهد الخليتين الآتيتين، هي:
(ZnIZn2+IICo2+ICo) Eo = 0.48 V , (MnIMn2+IICo2+ICo) Eo = 0.9 V
أ. Zn2+ أكثر ميلاً إلى الاختزال من Mn2+
ب. Zn2+ أكثر ميلاً إلى الاختزال من Co2+
ج. Co الأكثر ميلاً للتأكسد.
د. Mn2+ الأكثر ميلاً للاختزال.
3. خلية جلفانية قطباها (Cd,Pb)، وتتحرك فيها الأيونات السالبة من القنطرة الملحية نحو نصف الخلية (Cd2+|Cd). التفاعل الذي يحدث على المهبط، هو:
أ. Pb → Pb2+ + 2e-
ب. Cd → Cd2+ + 2e-
ج. Pb2+ + 2e- → Pb
د. Cd2+ + 2e- → Cd
4. إذا كان الفلز B يتفاعل مع محلول حمض الهيدروكلوريك HCl بينما لا يتفاعل الفلز E، ويمكن للوعاء المصنوع من الفلز A حفظ محاليل الفلزات B,C,E، بالإضافة إلى قدرة الفلز C على اختزال أيونات B2+، فإن ترتيب هذه الفلزات وفق قوتها بوصفها عوامل مختزلة، هو:
أ. A > B > E > C
ب. A > E > B > C
ج. A < E < B < C
د. A < B < E < C
5. إذا كان ترتيب الأيونات حسب جهد اختزالها هو D2+ > C2+ > B2+ > A2+، فإن الفلز الذي يمكنه استخلاص الفلزات الأخرى من محاليل أملاحها، هو:
أ. A
ب. B
ج. C
د. D
6. إذا كان التفاعلان الآتيان يحدثان تلقائيًا:
Zn + Cd2+ → Zn2+ + Cd
Cd + Sn2+ → Cd2+ + Sn
فإن ترتيب الأيونات (Cd2+, Zn2+, Sn2+) وفق قوتها بوصفها عوامل مؤكسدة، هو:
أ. Cd2+ < Zn2+ < Sn2+
ب. Cd2+ > Sn2+ > Zn2+
ج. Zn2+ < Cd2+ < Sn2+
د. Zn2+ > Cd2+ > Sn2+
7. اعتمادًا على جهود الاختزال المعيارية للفلزات المبينة في الجدول الآتي:

فإن الفلز الذي يمكنه تحرير غاز الهيدروجين (H2) من محلول الحمض HBr ولا يمكنه اختزال أيونات Co2+ هو:
أ. Cu
ب. Ni
ج. Cd
د. Al
8. 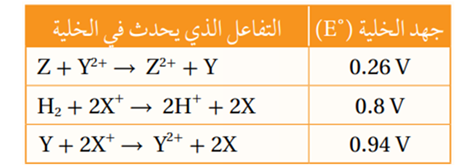 يبين الجدول الآتي قيم فرق الجهد الكهربائي لثلاث خلايا جلفانية. إذا علمت أن جهد اختزال الفلز R يساوي (-0.28V)، فإن الرمز الصحيح للخلية الجلفانية التي يمثل القطب R مهبطها، هو:
يبين الجدول الآتي قيم فرق الجهد الكهربائي لثلاث خلايا جلفانية. إذا علمت أن جهد اختزال الفلز R يساوي (-0.28V)، فإن الرمز الصحيح للخلية الجلفانية التي يمثل القطب R مهبطها، هو:
أ.R IY2+R2+lY
ب.R IX2+R2+lX
ج.R IZ2+R2+lZ
د.Z IR2+Z2+lR
إعداد : شبكة منهاجي التعليمية
27 / 03 / 2026
النقاشات