التهجين من نوع sp2
تجري الذرات المركزية تهجيناً من نوع sp2 إذا اختلط فلك من نوع s من الذرة المركزية، مع فلكين من نوع p من الذرة نفسها، فتتكون ثلاثة أفلاك مهجنة من نوع sp2 وتتجه الأفلاك المهجنة في الفراغ بحيث يكون التنافر بين إلكتروناتها أقل ما يمكن فتأخذ شكل مثلث مسوٍ والزاوية فيما بينها 120o
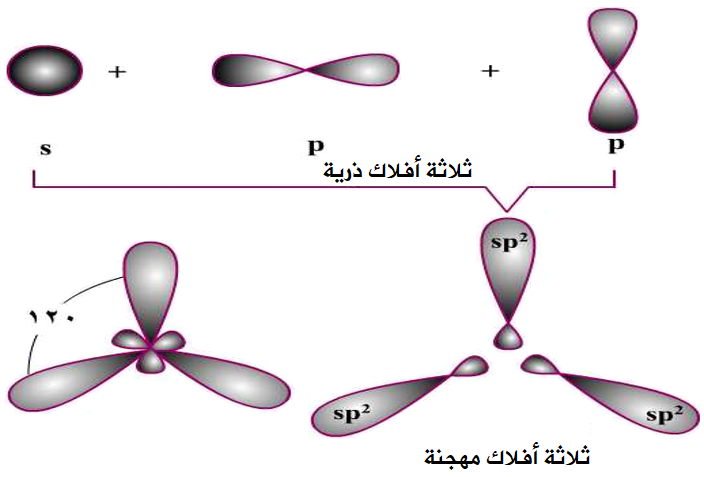
مثال: جزيء BCl3
انظر إلى التوزيع الإلكتروني لذرة البورون المركزية:
5B :[He] 2s2 2p1
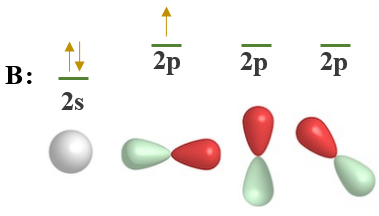
ومن التوزيع الإلكتروني تلاحظ أن ذرة البورون تحتوي على إلكترون منفرد، لذا فهي تميل للارتباط مع ذرة كلور واحدة، حسب نظرية رابطة التكافؤ، والتي تحدد من خلالها عدد الروابط من خلال عدد الإلكترونات المنفردة.
ولكي تربط ذرة البورون بثلاث ذرات كلور، يجب أن يكون لديها ثلاثة إلكترونات منفردة، وعليه تقوم ذرة البورون بعمل ترقية للإلكترون من المستوى الفرعي 2s إلى أحد أفلاك المستوى الفرعي 2p الفارغة.
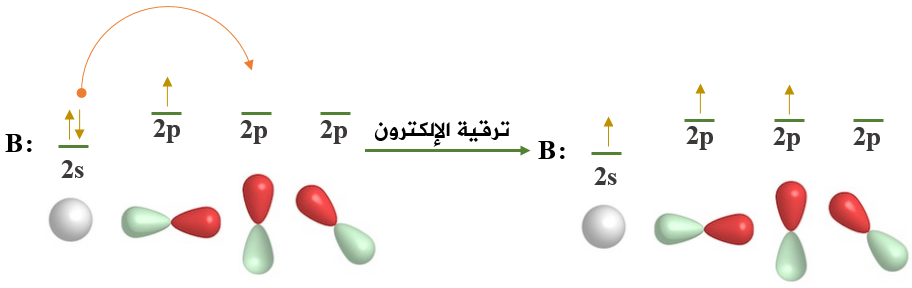
ولكي تكوّن ذرة البورون ثلاث روابط متكافئة مع ثلاث ذرات كلور تقوم بمساواة طاقة الأفلاك التي تحتوي على إلكترونات منفردة، وتخلطها معاً لتكوين ثلاثة أفلاك مهجنة يسمى كل واحد منهما sp2 ، مع بقاء فلك ذري فارغ من نوع 2p في ذرة البورون.
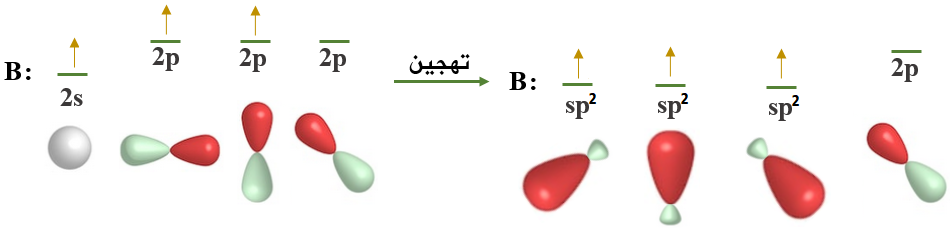
تتجه الأفلاك المهجنة في الفراغ بثلاث اتجاهات بحيث يكون التنافر بين إلكتروناتها أقل ما يمكن وتأخذ الأفلاك شكل مثلث مستوٍ، والزاوية 120o
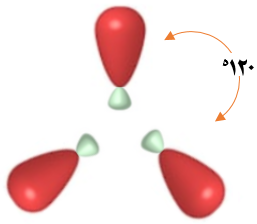
ثم تقدّم كل ذرة كلور فلكاً ذرياً من نوع 3p إلى كل فلك مهجن.
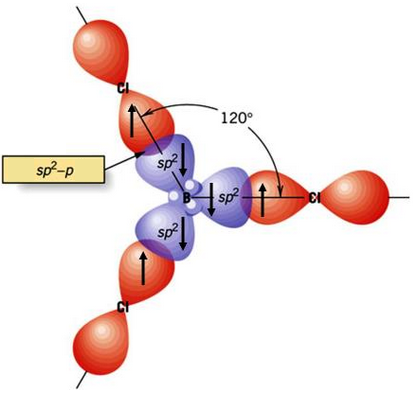
- نوع التهجين الذي تجريه ذرة البورون: sp2
- عدد الأفلاك المهجنة في ذرة البورون: 3
- الشكل الهندسي (البنائي) للجزيء: مثلث مستوٍ.
- قيمة الزاوية بين الأفلاك المهجنة: 120o
- نوع الأفلاك الداخلة في تكوين الرابطة sp2-p : B-Cl .
- مبرر التهجين: تفسير عدد الروابط.
إعداد : أ. أحمد الحسين
03 / 11 / 2022
النقاشات