التحليل الكهربائي
Electrolysis
مفهوم التحليل الكهربائي
التحليل الكهربائي: إحداث تفاعل التأكسد والاختزال نتيجة مرور تيار كهربائي في مصهور أو محلول مادة كهرلية.
وتسمى الدارة الكهربائية المستخدمة في ذلك، خلية تحليل كهربائي.
مفهوم خلية التحليل الكهربائي
خلية التحليل الكهربائي: الخلايا الكهركيميائية التي تتحول فيها الطاقة الكهربائية إلى طاقة كيميائية.
أجزاء خلية التحليل الكهربائي
- وعاء يحتوي على محلول أو مصهور مادة كهرلية.
- قطبان خاملان من الجرافيت لا يشتركان في التفاعل، إنما ينقلان الإلكترونات من المحلول أو المصهور الكهرلي وإليه، هما:
- المصعد (+): وتحدث عنده عملية التأكسد، ويتصل بالقطب الموجب للبطارية.
- المهبط (-): وتحدث عنده عملية الاختزال، ويتصل بالقطب السالب للبطارية.
- مصدر تيار (بطارية).

خطوات التحليل الكهربائي لمصاهير المواد الكهرلية
1- تعمل الحرارة على تفكيك المادة الكهرلية إلى أيونات موجبة وأخرى سالبة.
2- يتجه كل أيون إلى القطب المعاكس له في الشحنة.
3- يحدث اختزال للأيون الموجب عند المهبط (القطب السالب).
4- يحدث تأكسد للأيون السالب عند المصعد (القطب الموجب).
مثال (1):
التحليل الكهربائي لمصهور يوديد الرصاص PbI2
خطوات التحليل:
تعمل الحرارة على تفكيك يوديد الرصاص إلى أيونات رصاص موجبة، وأيونات كلوريد سالبة.
PbI2(s) Pb2+(l) + 2I-(l)
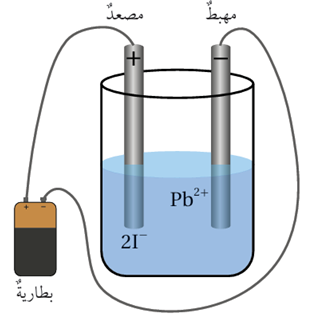 تتجه أيونات الرصاص الموجبة نحو المهبط (-) وتتعرض للاختزال بفعل الكهرباء القادمة من البطارية، وتتحول إلى ذرات الرصاص.
تتجه أيونات الرصاص الموجبة نحو المهبط (-) وتتعرض للاختزال بفعل الكهرباء القادمة من البطارية، وتتحول إلى ذرات الرصاص.
نصف تفاعل الاختزال / المهبط:
2Pb2+(l) + 2e- → Pb(s)
تتجه أيونات اليوديد السالبة نحو المصعد (+) وتتأكسد بفقد إلكترونات تعود إلى البطارية، وتتحول أيونات اليوديد إلى جزيئات يود.
نصف تفاعل التأكسد / المصعد:
2I-(l) → I2(s) + 2e-
التفاعل الكلي في خلية التحليل:
Pb2+(l) + 2I-(l) → Pb(s) + I2(s)
نواتج التحليل الكهربائي للمصهور:
- يتكون Pb على المهبط.
- يتكون I2 على المصعد.
مثال (2):
التحليل الكهربائي لمصهور بروميد البوتاسيوم KBr
خطوات التحليل:
تعمل الحرارة على تفكيك بروميد البوتاسيوم إلى أيونات بوتاسيوم موجبة، وأيونات بروميد سالبة.
KBr(s) K+(l) + Br-(l)
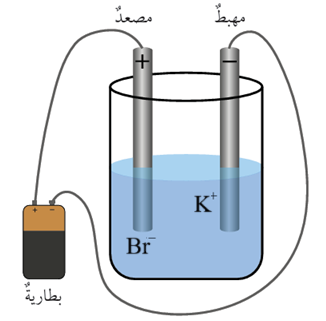 تتجه أيونات البوتاسيوم الموجبة نحو المهبط (-) وتتعرض للاختزال بفعل الكهرباء القادمة من البطارية، وتتحول إلى ذرات بوتاسيوم.
تتجه أيونات البوتاسيوم الموجبة نحو المهبط (-) وتتعرض للاختزال بفعل الكهرباء القادمة من البطارية، وتتحول إلى ذرات بوتاسيوم.
نصف تفاعل الاختزال / المهبط:
K+(l) + e- → K(s)
تتجه أيونات البروميد السالبة نحو المصعد (+) وتتأكسد بفقد إلكترونات تعود إلى البطارية، وتتحول أيونات البروميد إلى جزيئات بروم.
نصف تفاعل التأكسد / المصعد:
2Br-(l) → Br2(l) + 2e-
ولكتابة التفاعل الكلي في خلية التحليل، نضرب نصف تفاعل الاختزال في (2):
2K+(l) + 2e- → 2K(s)
التفاعل الكلي في خلية التحليل:
2K+(l) + 2Br-(l) → 2K(s) + Br2(l)
نواتج التحليل الكهربائي للمصهور:
- يتكون K على المهبط.
- يتكون Br2 على المصعد.
خطوات التحليل الكهربائي لمحاليل المواد الكهرلية
1- تتفكك المادة الكهرلية في الماء إلى أيونات موجبة وأخرى سالبة.
2- يتجه كل أيون إلى القطب المعاكس له في الشحنة.
3- يحدث اختزال للأيون الموجب أو الماء عند المهبط (القطب السالب).
تبعاً لسلسلة النشاط تختزل أيونات الفلزات قليلة النشاط وتترسب عند المهبط ولا تختزل جزيئات الماء.
H2O < Zn, Fe, Sn, Pb, Cu, Ag, Au
تبعاً لسلسلة النشاط تختزل جزيئات الماء ولا تختزل أيونات الفلزات عالية النشاط، وينتج عن اختزال الماء غاز الهيدروجين.
K, Na, Li, Ca, Mg, Al < H2O
4- يحدث تأكسد للأيون السالب أو الماء عند المصعد (القطب الموجب).
تتأكسد أيونات الهالوجينات السالبة وتتحول إلى جزيئات عند المصعد ولا تتأكسد جزيئات الماء.
H2O < Cl-, Br-, I-
تتأكسد جزيئات الماء، وينتج عن تأكسد الماء غاز الأكسجين، ولا أيونات المجموعات الأيونية.
NO3-, SO42- < H2O
مثال (1):
التحليل الكهربائي لمحلول بروميد النحاس CuBr2
خطوات التحليل:
يعمل الماء على تفكيك بروميد النحاس إلى أيونات نحاس موجبة، وأيونات بروميد سالبة.
CuCl2(s) Cu2+(aq) + 2Br-(aq)
تتجه أيونات النحاس الموجبة والماء نحو المهبط (-)، فتتعرض أيونات النحاس الموجبة للاختزال بفعل الكهرباء القادمة من البطارية، وتتحول إلى ذرات نحاس، ولا تختزل جزيئات الماء؛ لأن أيونات النحاس أسهل اختزالاً من الماء.
نصف تفاعل الاختزال / المهبط:
Cu2+(aq) + 2e- → Cu(s)
تتجه أيونات البروميد السالبة والماء نحو المصعد (+)، فتتأكسد بفقد إلكترونات تعود إلى البطارية، وتتحول أيونات البروميد إلى جزيئات بروم، ولا تتأكسد جزيئات الماء؛ لأن أيونات البروميد أسهل تأكسداً من الماء.
نصف تفاعل التأكسد / المصعد:
2Br-(aq) → Br2(l) + 2e-
نواتج التحليل الكهربائي للمحلول:
- يتكون Cu على المهبط.
- يتكون Br2 على المصعد.
مثال (2):
التحليل الكهربائي لمحلول كلوريد البوتاسيوم KCl
خطوات التحليل:
يعمل الماء على تفكيك كلوريد البوتاسيوم إلى أيونات بوتاسيوم موجبة، وأيونات كلوريد سالبة.
KCl(s) K+(aq) + Cl-(aq)
تتجه أيونات البوتاسيوم الموجبة والماء نحو المهبط (-)، فيختزل الماء بفعل الكهرباء القادمة من البطارية، ولا تختزل أيونات البوتاسيوم؛ لأن الماء أسهل اختزالاً من أيونات النحاس البوتاسيوم، ويتصاعد غاز الهيدروجين عند المهبط.
تتجه أيونات الكلوريد السالبة والماء نحو المصعد (+)، فتتأكسد بفقد إلكترونات تعود إلى البطارية، وتتحول أيونات الكلوريد إلى غاز الكلور، ولا تتأكسد جزيئات الماء؛ لأن أيونات الكلوريد أسهل تأكسداً من الماء.
نصف تفاعل التأكسد / المصعد:
2Cl- → Cl2 + 2e-
نواتج التحليل الكهربائي للمحلول:
- يتكون H2 على المهبط.
- يتكون Cl2 على المصعد.
إعداد : شبكة منهاجي التعليمية
30 / 03 / 2025
النقاشات