أسئلة مراجعة الوحدة الخامسة
السؤال الأول:
أوضح المقصود بكل مما يأتي:
- التفاعلات غير المنعكسة.
- اتزان ديناميكي.
- ثابت الاتزان.
- الاتزان غير المتجانس.
- ثابت تأين القاعدة الضعيفة.
السؤال الثاني:
أوضح: يتفاعل ثاني أكسيد الكبريت SO2 مع الكلور Cl2 وفق المعادلة الآتية:
SO2 (g) + Cl2 (g) SO2Cl2 (g) + Heat
أوضح أثر التغيرات الآتية على موضع الاتزان:
أ- زيادة تركيز Cl2 .
ب- سحب SO2Cl2 من الوعاء.
ج- تقليل كمية SO2 في وعاء التفاعل.
السؤال الثالث:
أتوقع أثر خفض درجة الحرارة على موضع الاتزان للتفاعلين المتزنين الآتيين:
أ- C2H4 (g) + H2O (g) C2H5OH (g) ΔH = -46 kJ
ب- N2 (g) + O2 (g) 2NO (g) ΔH = +90 kJ
السؤال الرابع:
أتوقع التفاعل الذي ينتج أكبر كمية من المواد عند زيادة الضغط الكلي المؤثر في وعاء التفاعل بين التفاعلات الآتية:
أ- PCl5 (g) PCl3 (g) + Cl2 (g)
ب- N2 (g) + 3H2 (g) 2NH3 (g)
ج- N2O4 (g) 2NO2 (g)
د- + 3H2 (g) CH4 (g) + H2O (g) CO (g)
السؤال الخامس:
أتنبأ بموضع الاتزان عند تقليل حجم الوعاء في العمليات الآتية مبرراً تنبؤاتي:
أ- تحلل المركب SO2Cl2 كما في المعادلة:
SO2Cl2 (g) SO2 (g) + Cl2 (g)
ب- تحضير الميثانول كما في التفاعل المتزن الآتي:
CO (g) + 2H2 (g) CH3OH (g)
ج- تفاعل ثلاثي كلوريد الفسفور PCl3 مع الأمونيا كما في المعادلة الآتية:
PCl3 (g) + 3NH3 (g) P(NH2)3 (g) + 3HCl (g)
السؤال السادس:
أطبق أكتب تعبير ثابت الاتزان لكل من التفاعلات الآتية:
أ- CaCO3 (s) CaO (s) + CO2 (g)
ب- 2N2O5 (g) 2N2O4 (g) + O2 (g)
ج- [Cu(H2O)4]2+ (aq) + 4NH3 (aq) [Cu(NH3)4]2+ (aq) + 4H2O (l)
د- HNO2 (aq) + H2O (l) NO2- (aq) + H3O+ (aq)
هـ- C5H5N (aq) + H2O (l) C5H5NH+ (aq) + OH- (aq)
السؤال السابع:
أفسر:
أ- لا يتأثر موضع الاتزان عند تغيير الضغط الكلي في وعاء التفاعل عند الاتزان للتفاعل الآتي:
CO (g) + H2O (g) CO2 (g) + H2 (g)
ب- يمكن زيادة كمية الناتج SCN- بترسيب أيونات الحديد Fe3+ من المحلول في التفاعل المتزن الآتي:
FeSCN2+ (aq) Fe3+ (aq) + SCN- (aq)
السؤال الثامن:
أحلل البيانات وأفسرها: يبين الجدول الآتي نتائج دراسة ثابت الاتزان لتفاعل ما عند درجات حرارة مختلفة، هل التفاعل ماص للحرارة أم طارد لها؟

السؤال التاسع:
تحضر الأمونيا NH3 بتسخين مزيج من غاز النيتروجين N2 وغاز الهيدروجين H2 عند ضغط معين، كما في المعادلة الآتية:
3N2 (g) + 3H2 (g) 2NH3 (g)
ضغطت كمية من غازي النيتروجين والهيدروجين إلى وعاء حجمه 10 L ، وسخنت إلى درجة حرارة 350 oC ؛ ليصل التفاعل إلى حالة الاتزان، حيث وجد أن عدد مولات النيتروجين والهيدروجين والأمونيا عند الاتزان تساوي: 1.5 , 5.75 , 4.25 على الترتيب.
أ- أحسب ثابت الاتزان للتفاعل عند 350 oC
ب- أقارن هذه النتائج بقيم ثابت الاتزان في الجدول رقم (1)، وأبرر هذا الاختلاف.
السؤال العاشر:
وجد أن ثابت الاتزان للتفاعل الآتي يساوي Kc = 4 x 1013 عند درجة 25 oC
2NO (g) + O2 (g) 2NO2 (g)
أ- أتوقع المواد المتوافرة بكمية أكبر في وعاء التفاعل عند الاتزان.
ب- أحسب تركيز NO2 عند يكون [NO] = [O2] = 2 x 10-6 M
السؤال الحادي عشر:
أطبق: يحدث التفاعل الآتي في وعاء مغلق حجمه 1 L
NO2 (g) + SO2 (g) NO (g) + SO3 (g)
أدخل mol 0.8 من الغازات الأربعة إلى وعاء التفاعل عند درجة حرارة معينة فوجد أن ثابت الاتزان للتفاعل عند درجة الحرارة نفسها يساوي 3.75 ، أحسب تراكيز هذه الغازات عند الاتزان.
السؤال الثاني عشر:
أطبق: يتحلل غاز بروميد اليود IBr وفق المعادلة الآتية:
2IBr (g) I2 (g) + Br2 (g)
إحدى التجارب جرى فيها تحليل 0.1 mol من بروميد اليود في وعاء حجمه 1 L عند درجة 100 oC ، وكان ثابت الاتزان يساوي 0.026 ، أحسب تراكيز المواد عند وصول التفاعل إلى حالة الاتزان.
السؤال الثالث عشر:
أحلل النتائج وأفسرها: تصنع الأمونيا بتسخين مزيج من غازي النيتروجين والهيدروجين بوجود عامل مساعد من معدن المغنتيت الصلب، كما في المعادلة الآتية:
3N2 (g) + 3H2 (g) 2NH3 (g) ΔH = -92 kJ
 ويبين الشكل المجاور نسبة الأمونيا الناتجة عند ظروف مختلفة من الضغط ودرجة الحرارة، أدرس المنحنى وأجيب عن الأسئلة الآتية:
ويبين الشكل المجاور نسبة الأمونيا الناتجة عند ظروف مختلفة من الضغط ودرجة الحرارة، أدرس المنحنى وأجيب عن الأسئلة الآتية:
أ- أفسر: أستخدم مبدأ لوتشاتيلييه لتفسير أثر زيادة درجة الحرارة على نسبة الأمونيا الناتجة.
ب- أفسر: أستخدم مبدأ لوتشاتيلييه لتفسير أثر زيادة الضغط على نسبة الأمونيا الناتجة.
ج- أكتب تعبير ثابت الاتزان للتفاعل باستخدام تراكيز المواد، وكذلك باستخدام الضغوط الجزئية للغازات.
السؤال الرابع عشر:
 أحلل النتائج: يبين الشكل المجاور النتائج التجريبية لخليط من الغازات (SO3 , SO2 , O2) عند الاتزان، أدرس الشكل وأجيب عن الأسئلة الآتية:
أحلل النتائج: يبين الشكل المجاور النتائج التجريبية لخليط من الغازات (SO3 , SO2 , O2) عند الاتزان، أدرس الشكل وأجيب عن الأسئلة الآتية:
أ- أحدد المنحنى الذي يمثل المواد المتفاعلة والمنحنى الذي يمثل المواد الناتجة.
ب- أكتب معادلة التفاعل الموزونة.
ج- أحسب ثابت الاتزان للتفاعل في ضوء هذه النتائج.
السؤال الخامس عشر:
تغطي الأسنان طبقة من المعادن تسمى طبقة المينا؛ تعمل على حماية الأسنان من التآكل.
أ- أسمي المعدن الأساسي التي تتكون منه هذه الطبقة.
ب- أوضح عملية إزالة المعدن وأكتب معادلة كيميائية تبين ذلك.
ج- أسمي المادة المستخدمة في إعادة بناء المعدن.
د- أوضح كيفية بناء المعدن في الأسنان.
السؤال السادس عشر:
اختار الإجابة الصحيحة لكل فقرة في ما يأتي:
1) أحدد التفاعل الذي يُنتج كمية أكبر من النواتج عند زيادة الضغط المؤثر على وعاء التفاعل:
أ- I2 (g) + Br2 (g) 2IBr (g)
ب- 2NH3 (g) N2 (g) + 3H2 (g)
ج- 2NO (g) + Br2 (g) 2NOBr (g)
د-+ 3H2 (g) CH4 (g) + H2O (g) CO (g)
2) يؤدي سحب غاز NH3 من وعاء التفاعل الآتي إلى:
4NH3 (g) + 5O2 (g) 4NO (g) + 6H2O (g)
أ- زيادة سرعة التفاعل الأمامي.
ب- زيادة إنتاج غاز NO
ج- إزاحة موضع الاتزان نحو اليمين.
د- إزاحة موضع الاتزان نحو اليسار.
3) يعد تحليل الماء إحدى طرق تحضير الهيدروجين كما في التفاعل الآتي:
2H2O (g) 2H2 (g) + O2 (g) ΔH = +48 kJ
أحدد أي الإجراءات الآتية يؤدي إلى زيادة كمية الهيدروجين الناتجة هو:
أ- زيادة درجة الحرارة.
ب- خفض درجة الحرارة.
ج- زيادة الضغط المؤثر.
د- إضافة كمية من غاز الأكسجين.
4) العبارة الصحيحة في ما يتعلق بالتفاعل عند الاتزان في ما يأتي:
أ- تراكيز المواد الناتجة مساوٍ لتراكيز المواد المتفاعلة.
ب- موضع الاتزان مزاح نحو تكوين المواد المتفاعلة.
ج- سرعة التفاعل الأمامي مساوية لسرعة التفاعل العكسي.
د- تعتمد قيمة ثابت الاتزان على التراكيز الابتدائية للمواد في التفاعل.
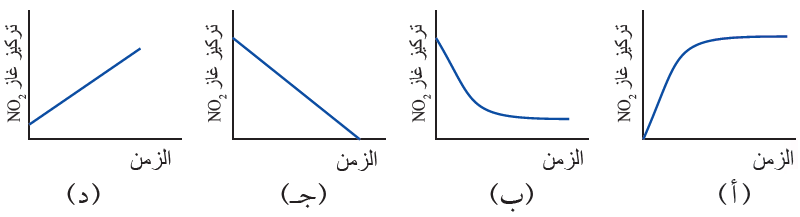
5) الشكل الذي يعبر عن تغير تركيز NO2 في أثناء سير التفاعل والوصول إلى حالة الاتزان للتفاعل الآتي هو:
NO2 (g) N2O4 (g)
إعداد : شبكة منهاجي التعليمية
06 / 05 / 2022
النقاشات